

近日,浙江泰林分析儀器有限公司自主研發的MD500型微生物快速檢測分析儀,不僅順利通過浙江省食品藥品檢驗研究院(以下簡稱“省藥檢院”)替代方法學權威驗證,更將這份驗證的嚴謹性與可靠性,成功落地終端客戶場景,獲得制藥企業質控團隊的高度認可,用硬核數據證明國產微生物快檢儀器的實力,為制藥行業微生物檢測合規升級注入新動能。
參考2025年版中國藥典四部指導原則《9201藥品微生物檢驗替代方法驗證指導原則》(以下簡稱指導原則9201),本次驗證針對激光誘導熒光檢測原理的MD500型微生物快速檢測分析儀,開展了專屬性、耐用性、準確度、精密度、線性、范圍和定量限等全參數驗證,驗證過程科學嚴謹、數據真實可靠。

一、儀器與試劑
儀器與設備

2.試驗菌株

3.培養基及試劑
胰酪大豆胨瓊脂培養基(TSA瓊脂)
R2A瓊脂
二、試驗方法
1.儲備用菌懸液制備
取保藏的各試驗菌,按既定驗證方案進行復蘇,并用純化水將新鮮培養物稀釋成約600 cfu/ml的菌懸液作為儲備用菌懸液。
2.儀器設置
MD500微生物快速檢測分析儀進樣模式為恒定流速模式,通過調節注射泵流速來控制菌液濃度。對于藥典組,則采用梯度稀釋的方法,使之達到與替代組一致的理論濃度。

三、驗證方案設計
替代組:取儲備用菌懸液,按既定泵速,采用MD500微生物快速檢測分析儀測定結果,每個濃度進行10次平行試驗。
藥典組:取儲備用菌懸液,按既定方案的稀釋方式將儲備用菌懸液稀釋為一定濃度的菌懸液,通過培養法進行藥典組檢測,每個濃度進行10次平行試驗。
陰性對照組:取100ml稀釋使用純化水,搖勻,全量過濾后抽干濾膜,取出濾膜貼至R2A 瓊脂,33 ℃培養5 d后計數。
四、線性和試驗范圍結果
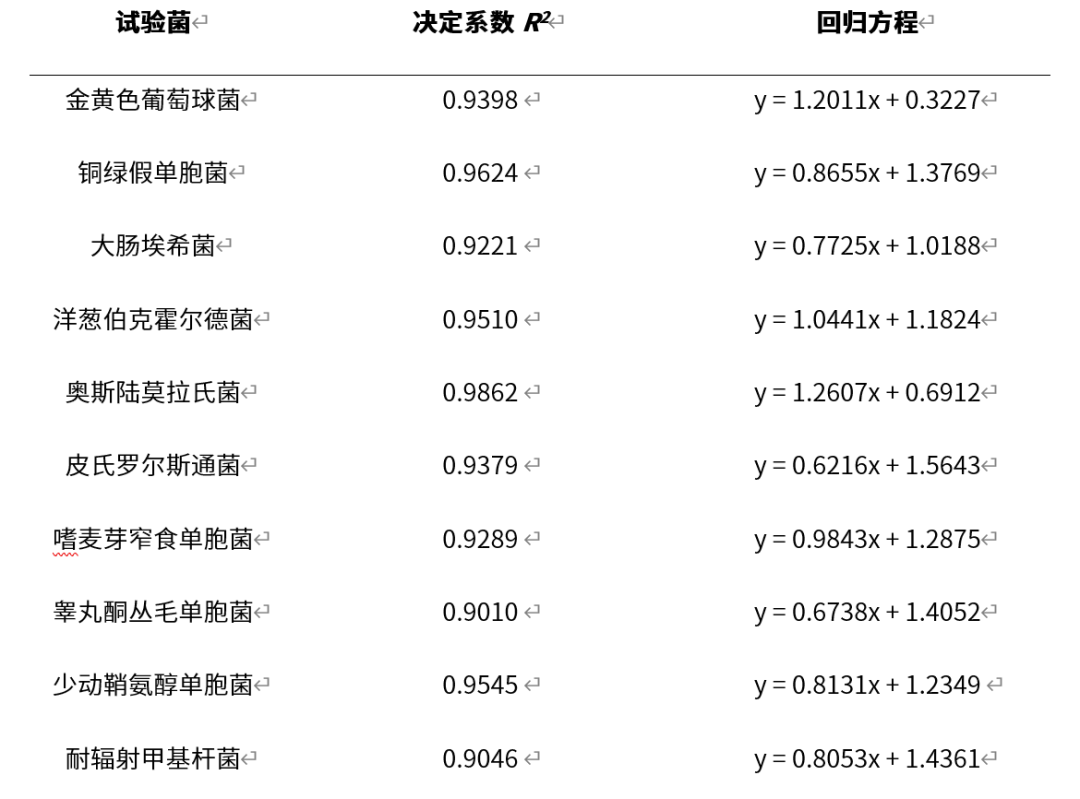
五、總結論
綜上所述,該替代方法的線性對于上述試驗菌在驗證范圍均不劣于藥典方法,范圍符合水系統微生物定量檢測的預期用途。
未來,浙江泰林分析儀器有限公司將持續深耕制藥質控領域,以更先進的技術、更嚴苛的品質、更完善的服務,打造更多符合行業需求的合規檢測解決方案,助力更多制藥企業實現微生物檢測的高效化、合規化、智能化升級,用國產技術力量護航醫藥行業高質量發展!
(篇幅有限,本文未收載驗證全部內容,如有疑問可咨詢浙江泰林分析儀器有限公司)


 EN
EN
